2026年3月18日,美国食品药品监督管理局(FDA)发布题为《药物开发中新方法论应用的通用考量》的行业指南草案,旨在为药物开发者提供一个验证框架,用于在药物开发中使用新方法论(NAMs),以改善对人体的毒性预测,逐步减少对动物试验的依赖。目前草案指南正面向公众征求意见,最终版将代表FDA的当前监管思路。

1、指南草案的发布背景
近年来,由于动物实验在预测人体反应方面的局限性、伦理关切以及高昂的成本,FDA正积极推动在药物非临床安全性评价中使用NAMs。据统计,超过90%在动物中显示安全有效的药物,最终因安全或疗效问题未能获得FDA批准。
关键政策节点如下(图1):
★ 2022年,美国国会通过了《FDA现代化法案2.0》
该法案取消了生物类似药申请中关于动物实验的要求,明确允许使用非动物替代方法支持新药临床试验申请和生物类似药许可申请。这项里程碑政策赋予FDA接受NAMs取代动物研究的权限。
★ 2025年4月,FDA发布《减少临床前安全性研究中动物实验的路线图》
计划引入计算建模及其他创新方法,以取代药物临床前安全性研究中的动物实验。通过鼓励药物申办方采用器官芯片、计算机建模、类器官及其他体外检测方法,FDA的目标是在3~5年内将动物实验减少到“例外而非常态”的程度。
★ 2026年3月,FDA又发布了《药物开发中新方法学应用的通用考量》草案
旨在为NAMs的验证和应用提供科学和监管框架。
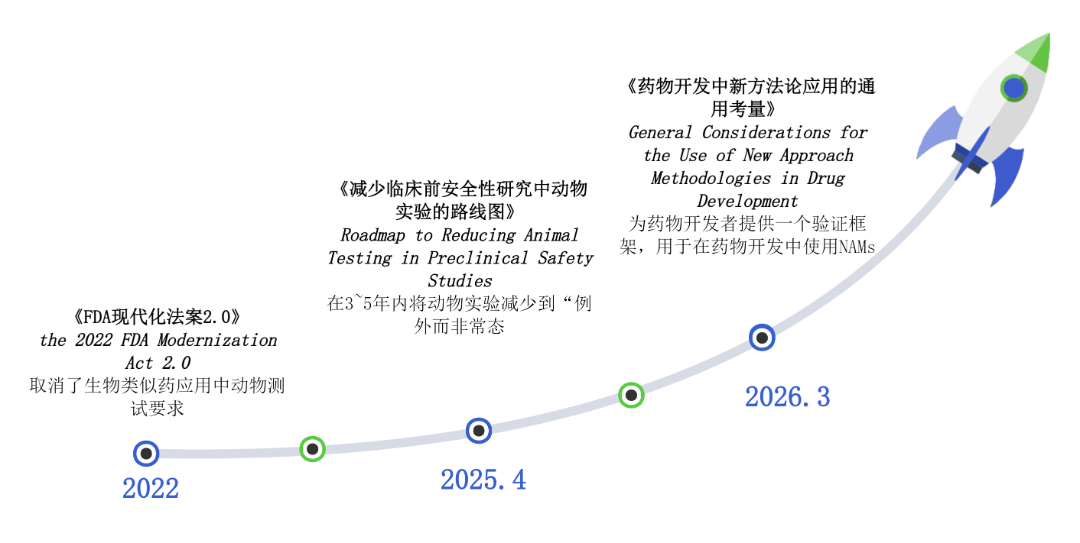
图1 美国FDA推行非动物替代试验关键节点
2 、指南草案的指导意义
《通用考量》草案的重大意义体现在以下几个关键方面:
(1) 建立科学共识与标准化:
为医药行业提供一个共同的“语言”和“质量标准”,使得NAMs数据具有可比性和可信度;
(2)明确监管期望,降低行业不确定性:
告知行业FDA会如何审评NAMs数据,以及什么样的证据更具说服力,是企业向FDA证明其NAMs数据可控的“操作手册”,降低企业的合规风险和创新障碍;
(3) 推动变革,激励创新:
FDA通过发布这份非强制的前瞻性指导,向行业发出“FDA支持并鼓励使用NAMs”的强烈信号,激励企业积极投资和探索NAMs技术,形成良性循环;
(4) 作为未来法规的“探路者”:
指导文件通常是法规变革的前奏,通过草案的实践和反馈积累经验,当技术和共识足够成熟时,有可能转化为正式的法规和标准。
3、NAMs的验证框架
为使NAMs数据能够用于监管决策,数据的可靠性和方法的可信度至关重要。《通用考量》草案提出了一个基于四个关键特征的框架,为计算毒理学工具的监管应用提供了清晰的验证路径:

以计算毒理学为引擎,赢取监管新赛道
从《FDA现代化法案2.0》到《路线图》,再到最新的《通用考量》草案,FDA正以清晰的步伐推动药物安全性评价从“动物依赖”转向“科学创新”。以计算毒理学为核心的NAMs策略,已成为药物研发与合规的必然选择。
对于企业而言,这既是挑战,更是构建差异化竞争力的机遇。谁能率先部署符合FDA标准的QSAR预测能力、建立规范化的Read-across评估流程、积累可复用的药物数据资产,谁就能在新规落地后的合规赛道上占据先机。
对企业的战略启示:以计算毒理学驱动合规转型
面对FDA这一系统性政策转向,合律曼从研发、合规、数据资产三个维度,合律曼为企业提出以下战略建议:
(1)前置计算毒理学,实现风险早期识别
传统“先合成、后测试”模式成本高昂且周期漫长。企业应在投入实验前,应用QSAR模型预测候选物的皮肤致敏性、眼刺激性、致癌性等关键终点;对于数据有限的物质,则通过Read-across策略,利用已知相似物的可靠数据填补评估缺口。
⭕合律曼价值:我们提供的计算毒理学预测服务,能够基于分子结构快速评估药物对主要靶器官的潜在风险,帮助企业在早期筛选出更安全的候选物,大幅降低后期因安全性问题导致的研发延误或合规风险。
(2)建立符合FDA标准的规范化评估流程
FDA指南明确要求NAMs需具备科学可靠性和相关性。对于QSAR模型,必须符合OECD五项验证原则:明确的终点、明确的算法、明确的适用范围、良好的预测能力、可能的机理解释。
⭕合律曼价值:我们依托专业毒理学团队,为企业提供符合OECD验证原则的QSAR预测报告、专家驱动的Read-across论证,以及整合计算预测、体外数据和AOP框架的证据权重分析,确保每一份报告都具备透明度、可追溯性和机理解释——这正是FDA审评的核心关注点。
(3)积累药物专属数据库,构建长期竞争壁垒
每一次合规评估产生的计算预测数据、Read-across论证逻辑及验证结论,都是企业宝贵的数字资产。高质量的数据积累是优化未来预测模型、支撑更复杂评估的基础。
⭕合律曼价值:我们的“数据生产-贸易准入-数据交易”三位一体服务模式,能够帮助企业建立结构化的药物安全数据仓库,构建企业专属的毒性数据库,支持内部快速筛查,在供应链谈判和产品生命周期管理中拥有无可争议的数据话语权。
❅参考文献
FDA pushes to replace animal testing. Nat Biotechnol 43, 655 (2025).
Fossler, M.J. and Garner, C.E. (2026), The FDA Roadmap to Reducing Animal Testing in Preclinical Safety Studies: Where Will It Lead Us? Clin Pharmacol Drug Dev, 15: e70046.
合律曼服务
✍️ QSAR建模服务
✍️ QSAR软件服务
✍️ COSMOS毒性预测
✍️ 化妆品原料信息报送
✍️ 化妆品注册备案
※ 版权声明:本文由合律曼数据整理,转载请注明出处!合律曼数据尊重知识产权,如内容涉及版权问题,烦请联系我们及时处理。合律曼数据随时为您更新化工新材料合规&数据跨境相关资讯,如有工业化学品REACH | 数据生产AI模型 | 数据标准与跨境交易 | 计算毒理QSAR | 全球SDS报告等相关问题欢迎咨询联系0571-86060701或点击下方图片在线咨询!
地址:浙江省杭州市拱墅区储鑫路21号网谷创新中心8幢903室
邮箱:info@compliancemen.com
QQ:3671987934

微信咨询

微信公众号
2012-2025 杭州合律曼数据服务有限公司版权所有 All Right Reserved 浙ICP备2025192110号-1 DESIGN BY WEETOP